近日,bat365在线平台官方网站、近海海洋环境科学国家重点实验室刘海鹏教授课题组在白斑综合征病毒(WSSV)免疫逃逸机制方面取得新进展,相关成果以“The crustacean DNA virus tegument protein VP26 binds to SNAP29 to inhibit SNARE complex assembly and autophagic degradation”为题,发表于病毒学知名期刊Journal of Virology.
该研究首次揭示了WSSV感染后表达的病毒蛋白如何逃逸自噬-溶酶体降解这一无脊椎动物抗病毒先天免疫的关键分子机制,阐明了WSSV结构蛋白VP26通过抑制自噬-溶酶体降解在促进病毒免疫逃逸中发挥核心作用�,为水生甲壳动物抗WSSV感染提供了新干预靶点。
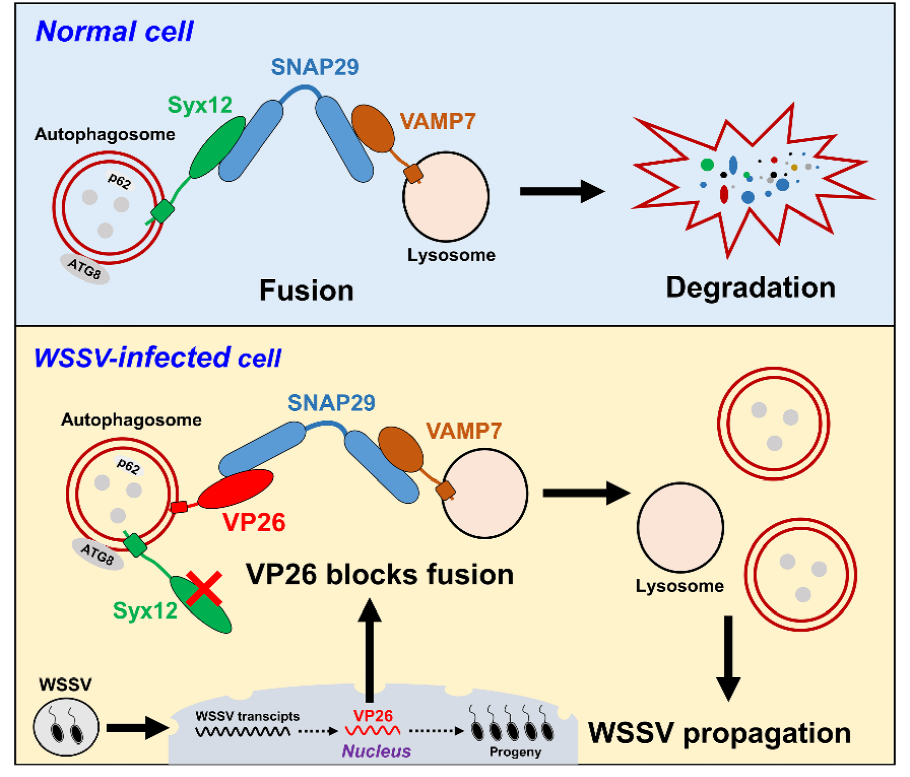
WSSV-VP26阻断SNARE复合体组装促进病毒逃逸
研究背景 Background
WSSV是目前危害虾类最严重的病毒性病原。不同于其他囊膜DNA病毒,WSSV子代病毒必须在宿主细胞核内完成�囊膜包被衣壳并组装成熟,然而,WSSV如何逃逸宿主细胞抗病毒先天免疫的关键分子机制仍不清楚。作为细胞抗病原感染先天免疫的重要组成部分,自噬�通常作为一种细胞监视机制来抵御入侵的病毒;同时,病毒也已进化出不同策略来抑制细胞自噬性降解等宿主关键抗病毒先天免疫反应,甚至策反细胞自噬以促进其子代病毒增殖。迄今为止,WSSV复制阶段如何逃逸宿主自噬性降解的关键分子机制尚不清楚。
团队前期研究发现,在WSSV感染早期阶段,内化入胞的病毒粒子巧妙地利用细胞内体系统进行胞质运输以逃逸自噬-溶酶体降解(Meng and Liu et al., Journal of Virology, 2020),并进一步劫持细胞核转运蛋白Importins(α1/β1)完成包裹有病毒基因组核衣壳的核靶向运输(Li and Liu et al., Journal of Virology, 2022)。在上述发现的基础上,为揭示WSSV感染后其新合成病毒蛋白如何逃逸宿主细胞自噬性降解的关键分子机制,该团队以红螯螯虾及其造血组织(Hpt)细胞为病毒感染模型,利用免疫荧光共聚焦显微镜、透射电镜、基因敲降、免疫共沉淀蛋白互作分析等分子生物学技术,阐明了WSSV结构蛋白VP26通过抑制介导自噬与溶酶体融合的SNARE复合物组装以协助WSSV逃逸宿主抗病毒先天免疫降解的关键分子过程。
研究结果 Research Results
研究发现,WSSV感染可明显增强螯虾Hpt细胞中的自噬标志物-内源性GB-II蛋白水平,且触发细胞内自噬体积累(图1)。自噬体积累是自噬流发生的中间过程,反映了自噬体形成以及自噬体与溶酶体融合形成自噬-溶酶体之间的平衡。因此,上述由WSSV感染诱发细胞中自噬体积累的原因存在两种可能:1)WSSV激活了自噬流;2)WSSV抑制了自噬体降解。

图1. WSSV感染触发细胞自噬体积累
为进一步阐明WSSV感染引发的自噬体积累属于哪种类型,研究人员择取经典自噬受体标志物p62予以分析:自噬流激活会消耗p62蛋白,导致其存量降低;反之,若自噬流被抑制,则会阻滞自噬降解进而导致p62蛋白累积。实验结果表明,WSSV感染后的p62蛋白与细胞内泛素化蛋白存量均显著增加(图2),这一结果表明WSSV感染明显抑制了宿主细胞的自噬性降解。
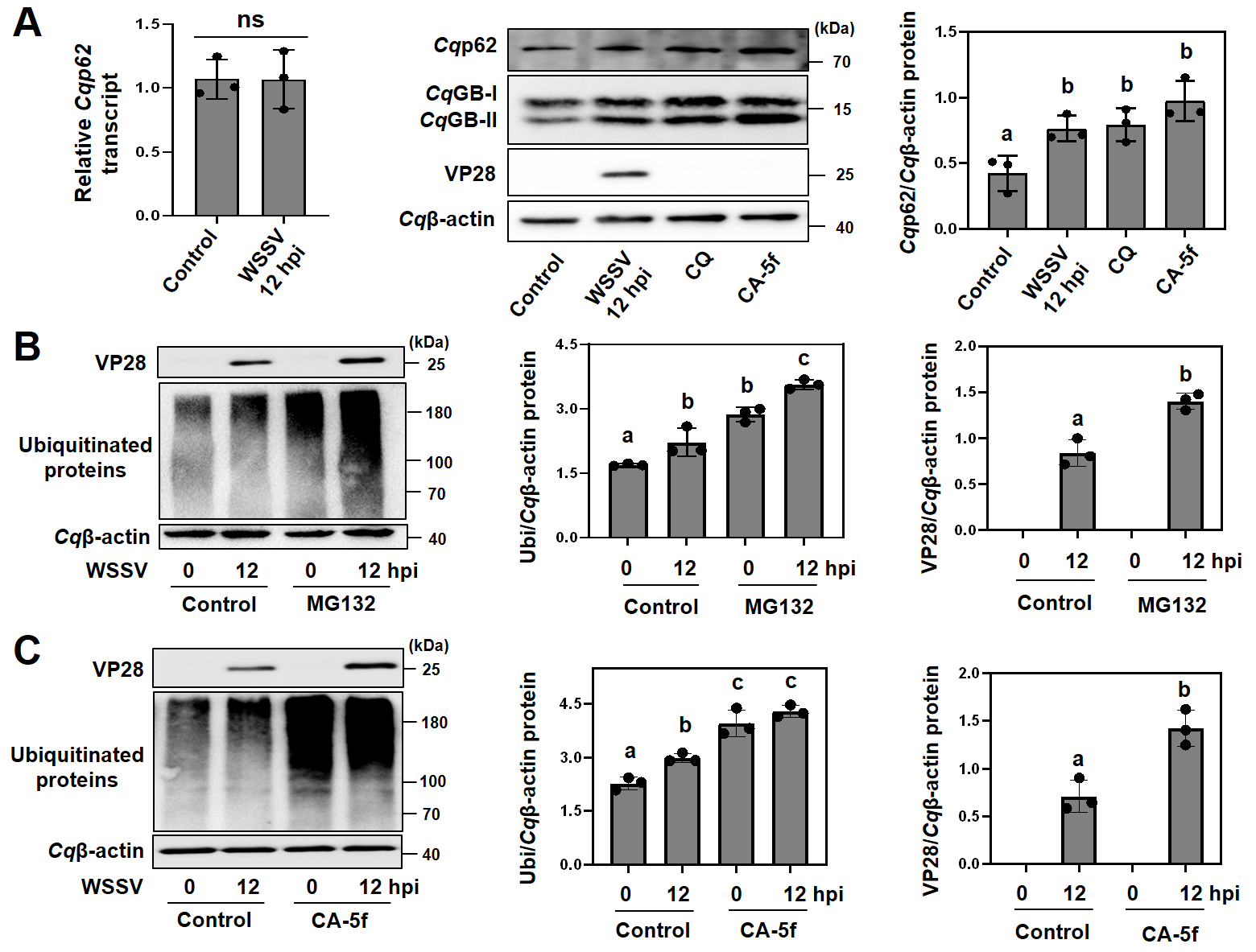
图2. WSSV感染抑制细胞自噬性降解
研究人员还就WSSV如何阻断细胞的自噬性降解进行了研究。通常情况下,自噬体需要与溶酶体融合形成自噬-溶酶体,以降解清除其包裹的微生物或细胞组分等“货物”;而介导自噬体与溶酶体融合的重要分子元件之一是可溶性N-乙基马来酰亚胺敏感因子附着蛋白受体(SNARE)复合体;基于此,研究人员针对“WSSV-SNARE复合物互作”开展研究。利用蛋白互作分析WSSV的5种主要结构蛋白与细胞的3种SNARE复合物因子,发现WSSV结构蛋白VP26可通过其C端区域识别结合SNARE复合体核心因子SNAP29,且VP26与SNAP29发生互作后会竞争性抑制自噬体Qa-SNARE Syx12蛋白结合胞质游离的Qbc-SNARE SNAP29蛋白,从而有效破坏SNARE复合物Syx12-SNAP29-VAMP7的组装(图3),进而抑制自噬体与溶酶体融合及其内容物的降解。

图3. WSSV-VP26抑制细胞SNARE复合物组装
此外,研究发现,WSSV-VP26利用其蛋白跨膜结构域锚定于细胞自噬体膜(图4),这种特异性定位很可能是WSSV-VP26靶向抑制自噬体与溶酶体融合的先决条件,从而抑制细胞自噬性降解过程(图4)以促进病毒免疫逃逸。

图4. WSSV-VP26跨膜区锚定于细胞自噬体膜抑制自噬性降解
综上所述,“WSSV-细胞自噬”博弈过程包含了复杂的多样性调控,上述发现为后续系统性探讨WSSV-宿主互作的关键调控网络机制奠定了基础。
研究团队及资助 Research Group and Funding
该论文第一作者为bat365在线平台官方网站博士后刘灵珂,通讯作者为刘海鹏教授。该研究获得国家自然科学基金(U2005210)、福建省海洋协同联盟项目(FOCAL2023-0106)、中央高校基本科研业务费专项资金(S202210384475, KFJJ-202215)的联合资助。
论文来源及链接
Liu L-K., Jian J-T., Jing S-S., Gao R-L., Chi X-D., Tian G., Liu H-P*. (2024). The crustacean DNA virus tegument protein VP26 binds to SNAP29 to inhibit SNARE complex assembly and autophagic degradation. Journal of Virology, e01408-23. doi: 10.1128/jvi.01408-23
https://journals.asm.org/doi/10.1128/jvi.01408-23
供稿:刘灵珂、刘海鹏
编辑:朱佳、苏颖
审核:林昕、张瑶、刘志宇、唐腾凤